Lernziele
Wenn Sie diese Seite durchgearbeitet haben, sollten Sie wissen
- Dass die theoretisch berechneten Produktverhältnisse nicht mit den experimentell ermittelten übereinstimmen müssen,
- dass tertiäre H-Atome leichter substituiert werden können als sekundäre, und diese wiederum leichter als primäre,
- dass der positive induktive Effekt von drei Alkylgruppen für die leichte Abspaltbarkeit tertiärer H-Atome verantwortlich ist.
Beispiel Propan
Auf der Vorseite hatten wir die Bromierung von Propan betrachtet und sind zu dem Schluss gekommen, das man ein Produktgemisch erhalten müsste, in dem hauptsächlich das 1-Brompropan vorkommt, und zwar zu 75%.
Wenn wir den Versuch aber tatsächlich durchführen könnten, erhielten wir ein völlig anderes, sehr überraschendes Ergebnis:
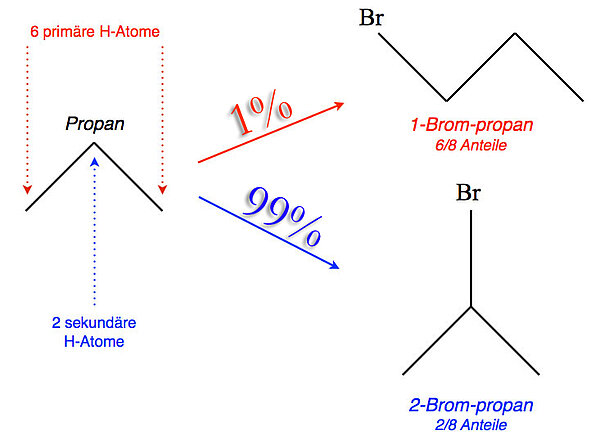
Das 2-Brompropan entsteht zu ca. 98 bis 99%, das 1-Brompropan nur zu 1 bis 2%. Das genaue Produktverhältnis hängt auch von der Temperatur ab, bei der der Versuch durchgeführt wird.
In der Stufe EF können wir dieses Ergebnis nur recht oberflächlich erklären, ein Jahr weiter in der Stufe Q1 packen wir das Thema etwas genauer an.
Einfache Erklärung
Propan enthält zwei Sorten von C-Atomen bzw. H-Atomen, nämlich primäre und sekundäre. Da unerwartet viel sekundäres 2-Brompropan entsteht, kann daraus eigentlich nur ein logischer Schluss gezogen werden: Die sekundären H-Atome können viel leichter durch Brom-Atome ersetzt werden als die primären H-Atome. Da aber alle H-Atome gleich sind, kann das nur an den C-Atomen liegen. Offensichtlich sind sekundäre C-Atome reaktiver als primäre, das heißt, man kann von einem sekundären C-Atom leichter ein H-Atom abspalten als von einem primären C-Atom.
Dass diese Vermutung korrekt ist, zeigen Versuche mit 2-Methylpropan oder 2-Methylbutan. Der Anteil an tertiärem Bromierungsprodukt ist noch höher als der Anteil an sekundärem Bromierungsprodukt, das heißt, ein tertiäres C-Atom ist noch reaktionsfreudiger als ein sekundäres.
Bessere Erklärung
Wenn man von einem C-Atom ein H-Atom homolytisch abspaltet, entsteht ein Alkyl-Radikal. Das C-Atom hat dann eine Kugelwolke, die nur mit einem Elektron besetzt ist, was energetisch recht ungünstig ist. Nach der Oktettregel werden stets zwei Elektronen pro Kugelwolke angestrebt.
Alkylgruppen, die mit diesem radikalischen C-Atom verbunden sind, haben einen sogenannten +I-Effekt, einen positiven induktiven Effekt. Das heißt, dass die Alkylgruppen Anteile ihrer Elektronendichte zum radikalischen C-Atom verschieben.
Die Elektronendichte an diesem C-Atom nimmt dadurch etwas zu, während die Elektronendichte in den Alkylgruppen etwas abnimmt. Das wirkt sich auch auf die einfach besetzte Kugelwolke des radikalischen C-Atoms aus. Rein rechnerisch gesehen befinden sich jetzt nicht 1,0 Elektronen in dieser Kugelwolke, sondern vielleicht 1,1 oder 1,2 Elektronen.
Die energetisch ungünstige Situation des Radikals wird also durch den positiven induktiven Effekt etwas abgemildert. Ein tertiäres Kohlenstoff-Radikal, das mit drei Alkylgruppen verbunden ist, ist also etwas stabiler als ein sekundäres Radikal, das nur mit zwei Alkylgruppen verbunden ist. Und das sekundäre Radikal ist stabiler als ein primäres, das nur mit einer einzigen Alkylgruppe verbunden ist. Am wenigsten stabil ist ein Methyl-Radikal; hier ist das radikalische C-Atom mit keinem weiteren C-Atom verbunden.
Eine noch bessere Erklärung setzt Grundkenntnisse des Orbitalmodells voraus. Der +I-Effekt der Alkylgruppen beruht auf einer Hyperkonjugation. Die p-Orbitale der radikalischen C-Atome überlappen etwas mit normalen kovalenten C-H-Bindungen, falls sich diese in günstiger Position befinden. Daher geben diese C-H-Bindungen etwas "Elektronendichte" an die einfach besetzten p-Orbitale ab, was deren energetische Lage etwas verbessert.
Aufgaben
Aufgabe 7
Bei der Bromierung von Alkanen werden - zumindest bei einer Temperatur von 100 ºC - tertiäre H-Atome 6.300 mal so leicht abgespalten wie primäre, und sekundäre H-Atome 250 mal so leicht wie primäre.
Das Propan-Molekül besitzt sechs primäre H-Atome und zwei sekundäre.
Versuchen Sie einmal, die Produktverhältnisse bei der Bromierung (100 ºC) möglichst genau zu berechnen. Wie viel Prozent 1-Brom-propan entsteht, und wie viel Prozent 2-Brom-propan?