Lernziele
Wenn Sie diese Seite durchgearbeitet haben, sollten Sie wissen
- Wie die Halogenierung eines Alkans Schritt für Schritt abläuft,
- welche Rolle dabei Radikale spielen,
- was man unter einer Startreaktion, einem Kettenfortpflanzungsschritt und einer Abbruchreaktion versteht,
- wie man die Reaktionsenthalpie einer solchen Reaktion berechnet.
Eine Kettenreaktion
Die Bromierung von Hexan erfolgt in mehreren Schritten. Damit wir aber nicht ständig sechs C-Atome mit ihren zugehörigen H-Atomen zeichen müssen, stellen wir hier den Mechanismus der Substitution an einem etwas einfacheren Beispiel vor. Wir wollen auf dieser Seite darstellen, wie Methan, das einfachste Alkan, bromiert wird.
KettenstartDer erste Schritt der Methan-Bromierung ist die Spaltung eines Brom-Moleküls. So ganz einfach ist die Spaltung eines Moleküls nicht, es muss ein ziemlicher Energiebetrag aufgewandt werden. Deswegen muss man den Erlenmeyerkolben bei der Bromierung von Hexan auch auf einen Tageslichtprojektor stellen oder mit einem Strahler belichten. Im Dunklen läuft die Reaktion nämlich nicht ab, zumindest nicht innerhalb einer Schulstunde.
Hier die Startreaktion:

Das Brom-Molekül wird durch energiereiches Licht homolytisch gespalten. Die Spaltung einer kovalenten Bindung durch Lichtenergie wird auch als Photolyse bezeichnet.
Die beiden Elektronen der kovalenten Bindung (blau hervorgehoben) verteilen sich gleichmäßig auf die beiden Spaltprodukte. Es entstehen zwei Brom-Atome. Jedes Brom-Atom besitzt drei doppelt besetzte Kugelwolken und eine Kugelwolke, die mit nur einem Elektron besetzt ist. Diese Kugelwolken wurden in der Zeichnung rot hervorgehoben.
Für Fortgeschrittene:
Wenn man den auf der ersten Seite beschriebenen Versuch so durchführt, dass man den Erlenmeyerkolben nur mit rotem Licht bestrahlt, dann dauert es sehr lange, bis eine Entfärbung auftritt. Bestrahlt man den Erlenmeyerkolben dagegen mit blauem Licht, läuft der Versuch sehr viel schneller ab. Das liegt daran, dass blaues Licht energiereicher ist als rotes Licht.
1. Kettenfortpflanzungsschritt
Die Brom-Atome mit ihrem ungepaarten Elektron sind nun extrem reaktiv. Eine Kugelwolke mit einem ungepaarten Elektron ist energetisch sehr ungünstig. Jede Kugelwolke strebt den Besitz von zwei Elektronen an. Daher werden Atome oder Moleküle mit einem solchen ungepaarten Elektron auch als Radikale bezeichnet, weil sie ein radikales chemisches Verhalten zeigen.
Wo soll das entstandene Brom-Radikal nun das fehlende Elektron her nehmen? Schauen wir uns dazu die Reaktionsgleichung des ersten Kettenfortpflanzungsschrittes näher an:

Wenn ein Brom-Radikal mit einem Methan-Molekül zusammenstößt, kann es passieren, dass das Brom-Radikal ein H-Atom samt Elektron aus dem Methan-Molekül "herausreißt". Dann hat das Brom-Atom sein zweites Elektron, allerdings hat es sich dabei auch ein H-Atom eingefangen. Aus dem Brom-Radikal ist ein HBr-Molekül enstanden.
Das Methan-Molekül hat jetzt ein H-Atom an das Brom-Atom verloren. Aus dem Elektronenpaar, welches das H-Atom mit dem zentralen C-Atom verbunden hatte, ist ein ungepaartes Elektron geworden. Aus dem Methan-Molekül ist ein Methyl-Radikal geworden. Das eine Radikal (Br*) ist also durch ein anderes Radikal (*CH3) ersetzt worden; die Zahl der Radikale hat sich bei diesem Schritt nicht erhöht.
Das Methyl-Radikal ist nun selbst in einem energetisch ungünstigen Zustand, weil es eine Kugelwolke mit nur einem Elektron besitzt. Was passiert nun?
2. KettenfortpflanzungsschrittStößt das Methyl-Radikal auf ein Brom-Molekül, so passiert folgendes:

Das Methyl-Radikal reißt ein Brom-Atom aus einem Br2-Molekül heraus und übernimmt dabei eines der beiden Bindungselektronen der Br-Br-Bindung. Aus dem Methyl-Radikal wird ein Brommethan-Molekül, und übrig bleibt ein neues Brom-Radikal. Und wieder ist ein Radikal durch ein anderes Radikal ersetzt worden, die Zahl der Radikale erhöht sich nicht.
Das entstandene neue Brom-Radikal kann nun wieder mit einem Methan-Molekül reagieren, und dann sind wir wieder beim ersten Kettenfortpflanzungsschritt. Dort entsteht ein neues Methyl-Radikal, dass dann wieder mit einem Brom-Molekül zu Brommethan und einem weiteren Brom-Radikal reagiert.
Und so geht das viele Hundert oder sogar Tausend Male weiter, bis es irgendwann zu einem Kettenabbruch kommt, weil zwei Radikale zusammenstoßen und ein Molekül bilden.
KettenabbruchEin Kettenabbruch findet immer dann statt, wenn zwei dieser Radikale zusammenstoßen.
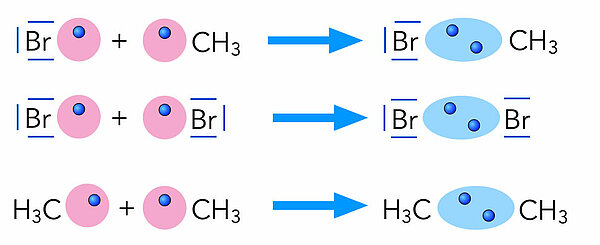
Das können zwei Brom-Radikale sein, wobei sich ein Brom-Molekül bildet. Oder ein Brom-Radikal stößt mit einem Methyl-Radikal zusammen, so dass sich Brommethan bildet. Oder aber zwei Methyl-Radikale vereinigen sich zu einem Ethan-Molekül. Tatsächlick kann man bei der Umsetzung von Brom mit Methan geringe Spuren von Ethan als Nebenprodukt nachweisen.
Aufgaben
Aufgabe 1
Erklären Sie die Tatsache, dass bei der Bromierung von Methan auch geringe Spuren von Bromethan als Nebenprodukt auftreten.
Aufgabe 2
Betrachten Sie die Tabelle mit den Bindungsdissoziationsenergien auf der Lexikon-Seite "Bindungsdissoziationsenergie".
Berechnen Sie die Energiebilanz des ersten Kettenfortpflanzungsschritts der Hexan-Bromierung
a) Für den Fall, dass ein primäres H-Atom substituiert wird,
b) für den Fall, dass ein sekundäres H-Atom substituiert wird.
Tipp: Auf der Seite "Bindungsdissoziationsenergie" finden Sie zwei Tabellen. Sie müssen für diese Aufgabe beide Tabellen heranziehen!
Aufgabe 3
Auch für diese Aufgabe benötigen Sie die beiden Tabellen mit den Bindungsdissoziationsenergie. Die Gesamtgleichung der Hexan-Bromierung lautet
$C_{6}H_{14} + Br_{2} \to C_{6}H_{13}Br + HBr$
Falls der Browser die Formeln auf dieser Seite nicht richtig darstellt, wurde die Erweiterung MathJax nicht korrekt geladen. Entweder ist der Browser veraltet, oder es besteht im Augenblick keine Internetverbindung.
Berechnen Sie die Energiebilanz der Hexan-Bromierung
a) Für den Fall, dass ein primäres H-Atom substituiert wird,
b) für den Fall, dass ein sekundäres H-Atom substituiert wird.
Aufgabe 4
Begründen Sie, wieso die Reaktionsenthalphie der Startreaktion sowie der Kettenabbruchreaktionen bei der Berechnung der Gesamtenergiebilanz keine Rolle spielen.
Aufgabe 5
Auch für diese Aufgabe benötigen Sie die beiden Tabellen mit den Bindungsdissoziationsenergie.
Die Energiebilanz für die Hexan-Bromierung hatten Sie ja bereits in Aufgabe 3 berechnet. Berechnen Sie nun bitte auch die Energiebilanz für die Fluorierung, Chlorierung und Iodierung von Hexan, unter der Annahme, dass ein sekundäres H-Atom substituiert wird.