Voraussetzungen
Wenn Sie diese Seite erfolgreich durcharbeiten wollen, sollten Sie folgende Fragen schon beantworten können:
- Was ist der Unterschied zwischen einer monomolekularen und einer bimolekularen Reaktion?
Lernziele
Wenn Sie diese Seite durchgearbeitet haben, sollten Sie wissen
- dass nucleophile Substitutionen monomolekular oder bimolekular ablaufen können,
- dass man entsprechend zwischen SN1-Reaktionen und SN2-Reaktionen unterscheiden kann.
Erstes Beispiel
Chlormethan CH3Cl reagiert mit Natronlauge NaOH bei erhöhter Temperatur zu Methanol CH3OH und Natriumchlorid NaCl:
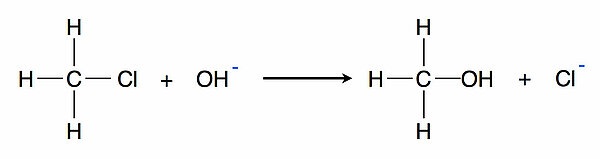
Die Natrium-Ionen können bei dieser Reaktion vernachlässigt werden, sie spielen nur eine Rolle als Gegenkationen für das Nucleofug (die Austrittsgruppe) Cl-.
Untersucht man nun die Kinetik dieser Reaktion, so stellt man fest, dass die Reaktionsgeschwindigkeit sowohl von der Konzentration des Substrats Chlormethan wie auch von der Konzentration des Nucleophils OH- abhängt:
vR = k * c(CH3Cl) * c(NaOH)Es handelt sich also um eine bimolekulare Reaktion bzw. um eine Reaktion 2. Ordnung. Beide Edukt-Teilchen, also sowohl die CH3Cl-Moleküle wie auch die OH--Ionen, müssen aufeinanderprallen, damit es zu einem erfolgreichen Zusammenstoß kommt.
Zweites Beispiel
Kommen wir auf den Versuch zurück, der auf der Vorseite vorgestellt wurde. Wenn wir 2-Brom-2-methylpropan und Ethanol in Anwesenheit von Silbernitrat zusammengeben, beobachten wir eine intensive Reaktion.
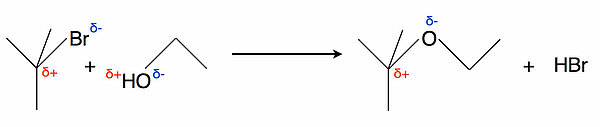
Aus Ethanol und 2-Brom-2-methylpropan bilden sich ein Ethyl-butyl-ether und Bromwasserstoff. An sich könnte man hier nicht viel beobachten. Aber das Silbernitrat reagiert mit den ausgetretenen Bromid-Ionen bzw. mit den von den HBr-Molekülen abgegebenen Bromid-Ionen zu wasserunlöslichem Silberbromid, und die Entstehung dieses Salzes kann man sehr gut beobachten.
Untersucht man die Kinetik dieser Reaktion, so stellt man fest, dass die Reaktionsgeschwindigkeit nur von der Konzentration des Substrats 2-Brom-2-methylpropan abhängt, nicht aber von der Konzentration des neutralen Nucleophils C2H5-OH:
vR = k * c((CH3)3Br)Es handelt sich also um eine monomolekulare Reaktion bzw. um eine Reaktion 1. Ordnung.
SN1- und SN2-Reaktionen
Grundsätzlich kann man zwei verschiedene Kinetiken bei nucleophilen Substitutionen beobachten. Manche Reaktionen laufen monomolekular ab, andere bimolekular. Entsprechend unterscheidet man SN1-Reaktionen und SN2-Reaktionen. Ob eine bestimmte nucleophile Substitution nach den SN1- oder nach dem SN2-Mechanismus abläuft, hängt von vielen Faktoren ab. Das Substrat, das Nucleophil, aber auch die Temperatur, das Lösemittel und andere Faktoren spielen hier eine Rolle.
Jetzt wissen wir natürlich immer noch nicht, was genau bei einer SN2-Reaktionund bei einer SN1-Reaktiongeschieht. Das wird aber auf den nächsten Seiten geklärt.
Quellen:
- Vorlesung Organische Chemie 1.17 von Prof. G. Dyker: "Nucleophile Substitution" (YouTube)
- Römpp Chemie-Lexikon, 9. Auflage 1992
- Morrison/Boyd, Organic Chemistry, 7th Edition, 2011
- Carey/Sundberg, Organische Chemie - ein weiterführendes Lehrbuch, Weinheim 1995