Die Austrittsgruppe
Nicht alle Abgangs- oder Austrittgruppen (Nucleofuge) lösen sich leicht von ihrem C-Atom. Wenn durch die Abspaltung einer nucleofugen Gruppe ein besonders stabiles Anion entsteht, ist das sowohl für die SN1 wie auch für die SN2-Reaktion günstig. Ein gutes Beispiel für eine solche Gruppe ist die SO3H - Gruppe bzw. das entsprechende Anion. Warum ist diese Gruppe eine gute Abgangsgruppe? Das liegt daran, dass die negative Ladung des Nucleofugs durch Mesomerie stabilisiert werden kann:
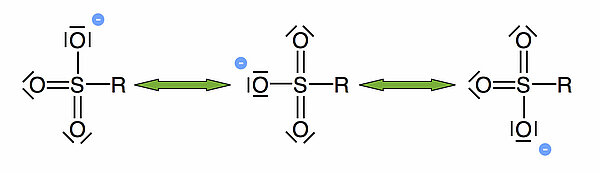
Als gute Austrittsgruppe gilt auch das Iod-Atom, während das Chlor-Atom eher eine schlechte Austrittsgruppe ist.
Allgemein gilt für die "Güte" oder "Eignung" einer Gruppe als Nucleofug folgende Reihenfolge:
I- > Br- > Cl- > F-
Das entspricht genau der Stärke der Nucleophile im Lösemittel Wasser, was bereits unter "Einfluss des Lösemittels" ausgeführt wurde. Auch die OH-Gruppe ist eine schlechte Abgangsgruppe. Aber durch Protonierung kann man aus dieser schlechten Abgangsgruppe eine gute Abgangsgruppe machen.
Experimentell beweisen kann man diese Reihenfolge, indem man Halogenalkane mit einem Nucleophil reagieren lässt, die neben einem Brom-Atom auch ein Iod-Atom besitzen. In der Regel wird dann das Iod-Atom substituiert, während das Brom-Atom im Molekül verbleibt.
Auch das Lösemittel spielt eine wichtige eine Rolle dabei, ob ein Nucleofug eine gute Austrittsgruppe ist. Kann das Lösemittel beispielsweise H-Brücken mit dem Nucleofug bilden, so wird der Austritt erleichtert und der Wiedereintritt erschwert (die Rückreaktion wird also behindert).
Wenn die Austrittsgruppe bzw. das abgegebene Anion gleichzeitig eine starke Brönsted-Base ist, so kann leicht eine Eliminierung als Konkurrenzreaktion stattfinden. Das ausgetretene Nucleofug holt sich dann nämlich ein Proton aus dem organischen Edukt, dabei entsteht dann eine C=C-Doppelbindung.
Die Austrittsgruppe als NucleophilNachdem die nucleophile Substitution erfolgt ist, liegt die Austrittsgruppe als Anion in der Lösung vor. Jetzt kann natürlich eine Rückreaktion einsetzen, bei der das Anion als Nucleophil fungiert. Ist das Anion ein starkes Nucleophil, wird die Rückreaktion begünstigt.
Iodid-Ionen sind sehr starke Nucleophile, daher sollte man erwarten, dass Iod-Alkane so gut wie nicht nucleophil substituiert werden können. Gelänge es einem Nucleophil, das Iod-Atom aus dem Substrat zu verdrängen, dann wären sofort viele Iodid-Ionen in der Lösung, die das Produkt dann wieder nucleophil angreifen würden. Dennoch gilt Iod als ein sehr gutes Nucleofug, das leicht verdrängt werden kann.
Wenn man das Gleichgewicht der Reaktion nach rechts verschieben will, sind Silber-Ionen sehr hilfreich. Diese verbinden sich mit den abgespaltenen Iodid-Ionen zu unlöslichem Silberiodid und entziehen dieses Endprodukt somit dem Gleichgewicht. Das funktioniert natürlich nicht, wenn man das Iod durch Chlor oder Brom substituieren will, weil die Silber-Ionen dann die Chlorid- oder Bromid-Ionen abfangen würden. Aber bei Nucleophilen, die mit Silber-Ionen keine Salze bilden, funktioniert das Verfahren.