Dehydrierung von Alkanen
Dieses Verfahren spielt bei der industriellen Synthese von Alkenen eine große Rolle. Alkane können problemlos aus dem Erdgas oder dem Erdöl gewonnen werden, aus dem Erdöl i.d.R. durch fraktionierte Destillation. Durch das sogenannte Cracken können längere Alkane in kurzkettige Alkane und Alkene gespalten werden. Dass bei diesem Cracken Alkene entstehen müssen, zeigt schon eine einfache mathematische Überlegung. Nehmen wir mal an, wir hätten das Alkan Pentan C5H12 zur Verfügung und spalten dieses in zwei Bruchstücke mit zwei bzw. drei C-Atomen auf. Die 12 H-Atome müssen nun auf die beiden C-Körper verteilt werden. Wenn nun Ethan C2H6 entsteht, bleiben nur noch 3 C-Atome und 6 H-Atome übrig. Als zweites Reaktionsprodukt kann dann nur noch Propen C3H6 entstehen.
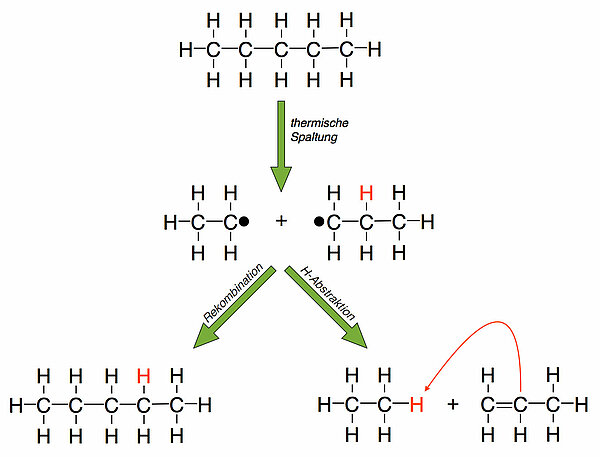
Bei der sogenannten Pyrolyse werden Alkane unter Einwirkung eines Katalysators (Zeolith) erhitzt, dabei bilden sich kürzere Alkylradikale. Solche Alkylradikale haben zwei Möglichkeiten, miteinander zu reagieren. Zunächst einmal kann sich ein neues, größeres Alkan aus zweien dieser Radikale bilden (linker Reaktionsweg). Zum andern kann ein Radikal ein H-Atom homolytisch abspalten und auf das andere Radikal übertragen (Wasserstoff-Abstraktion). So entstehen ein Alkan und ein Alken (rechter Reaktionsweg). Beim thermischen Cracken laufen übrigens ähnliche Prozesse ab: Lange Alkane werden durch hohe Temperaturen in kurze Alkylradikale gespalten, die dann auf die oben gezeigte Weise zu kürzeren Alkanen oder Alkenen reagieren. Natürlich entstehen dabei durch Rekombination von Radikalen auch wieder Moleküle längerer Alkane, aber diese können dann wieder durch die hohe Temperatur in zwei neue Alkylradikale gespalten werden.
Dehydratisierung von Alkoholen
Alkohole können leicht dehydratisiert werden, wobei sich dann Alkene bilden. Entzieht man beispielsweise Ethanol eine OH-Gruppe und ein H-Atom (also ein Wasser-Molekül = Dehydratisierung), dann bildet sich Ethen. Die Reaktion kann in einem einfachen Schulversuch durchgeführt werden. Dazu wird allerdings konz. Schwefelsäure als Katalysator benötigt.
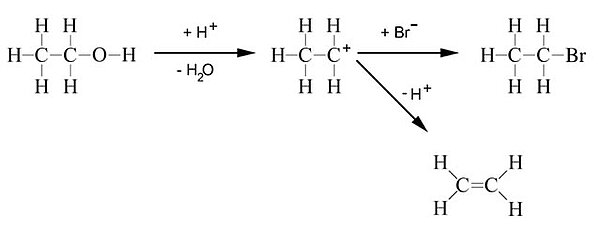
Wie man auf dem Bild gut sehen kann, ist die Dehydratisierung eine Eliminierungsreaktion, die in Konkurrenz zur Nucleophilen Substitution (SN1) abläuft. Auf der Seite "Alkohole: Dehydratisierung" der Chemgapedia findet sich ein schöner Videofilm, der die Eliminierung von Wasser aus Cyclohexanol zeigt. Industriell bedeutsam ist die Dehydratisierung von Alkohol in Ländern mit großer Bioethanol-Produktion, zum Beispiel Brasilien, Kolumbien oder USA.
Eine industriell bedeutsame Dehydratisierung ist laut Chemgapedia die Synthese von 1,3-Butadien aus 1,4-Butandiol:

In der Wikipedia dagegen wird diese Synthese nicht erwähnt. Dort wird geschrieben, dass 1,3-Butadien hauptsächlich durch Cracken von gesättigten Kohlenwasserstoffen hergestellt wird.
Die Dehydratisierung von Alkoholen ist laut Morrison/Boyd (Organic Chemistry, 7th Edition, 2014) neben der Dehydrohalogenierung von Halogenalkanen die wichtigste Methode zur präparativen Darstellung ("methods of preparation") von Alkenen.
Dehydrohalogenierung von Halogenalkanen
Ähnlich wie die Dehydratisierung von Alkoholen läuft Eliminierung von Halogenwasserstoff aus Halogenalkanen ab. Aus Chlorethan beispielsweise kann man durch Abspaltung von HCl Ethen herstellen. Während die Abspaltung von Wasser (Dehydratisierung, siehe oben) eine saure Katalyse erfordert, verläuft die Abspaltung einer Säure wie HCl oder HBr und basischer Katalyse. Das ist ja auch irgendwie logisch. Der entscheidende Schritt bei dieser Eliminierung ist die Abspaltung eines Protons aus dem Halogenalkan. Das gelingt nur, wenn eine starke Base anwesend ist, die bereit ist, das Proton aufzunehmen. Gleichzeitig mit der Abspaltung des Protons wird das Halogenid-Ion abgespalten.
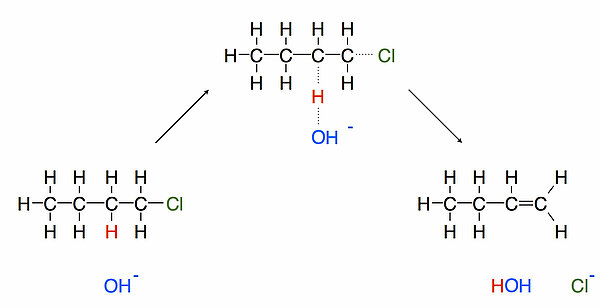
Hier sieht man die Reaktion mit dem Übergangszustand, in dem das H-Atom noch halb mit dem Halogenalkan verbunden ist, aber gleichzeitig auch schon halb mit der Base. Das entstandene Wasser-Molekül gibt dann ein Proton an das Chlorid-Ion ab, so dass HCl als Nebenprodukt entsteht. Dabei wird das am Anfang benötigte Hydroxid-Ion wieder frei. Es handelt sich also um eine echte basische Katalyse, die OH--Ionen werden nicht verbraucht.
Dehalogenierung von vicinalen Dihalogenalkanen
Aus sogenannten vicinalen Dihalogeniden kann mit Hilfe des unedlen Metalles Zink leicht ein Halogen-Molekül abgespalten werden. Vicinale Dihalogenide sind Dihalogenalkane, bei denen die beiden Halogen-Atome an benachbarten Kohlenstoff-Atomen sitzen. Auch diese Reaktion ist eine Eliminierung.
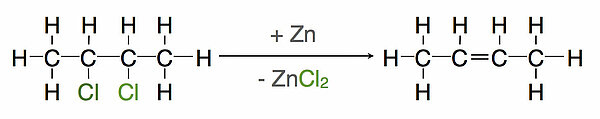
Reduktion von Alkinen
Dieses Verfahren soll nur der Vollständigkeit halber erwähnt werden. Versetzt man ein Alkin mit Wasserstoff, so kann sich mit Hilfe von Katalysatoren das entsprechende Alken bilden. Wenn man nicht aufpasst, hat man natürlich gleich das entsprechende Alkan.
Reduktion von Aldehyden und Ketonen
Auch dieses Verfahren soll nur der Vollständigkeit halber erwähnt werden. Aldehyde und Ketone können mit geeigneten Reagenzien und unter Einwirkung von Katalysatoren zu Alkenen reduziert werden. Bekannte Syntheseverfahren sind hier die Wittig-Reaktion, die Peterson-Reaktion und die Shapiro-Reaktion, auf die ich hier aber nicht eingehe, sondern stattdessen auf die entsprechenden Wikipedia-Artikel verweise.
Zusammenfassung: Darstellung von Alkenen
