Definition
Halogenalkane sind Alkane, bei denen ein oder mehrere Wasserstoff-Atome durch Halogen-Atome ersetzt worden sind. Die Halogenalkane werden oft auch als Alkylhalogenide bezeichnet, so zum Beispiel im Römpp Chemie-Lexikon[1].
Neben monosubstituierten Halogenalkanen wie zum Beispiel Chlorethan gibt es auch mehrfachsubstituierte Halogenalkane wie Trichlormethan (Chloroform). Halogenalkane können auch verschiedene Halogene enthalten, beispielsweise Fluor und Chlor gleichzeitig (FCKWs).

Das Bild oben zeigt vier typische Halogenalkane.
Chloroform wurd 1831 zum ersten Mal hergestellt. Anfänglich wurde es als Betäubungsmittel verwendet, ist aber wegen seiner gravierenden Nebenwirkungen schon lange als solches abgelöst worden.
2-Chlor-2-methylpropan ist ein wichtiges Reagenz in der industriellen Chemie. Es dient bei Synthesen zur Einführung einer tert-Butylgruppe in organische Moleküle[1].
2-Brom-2-fluorbutan ist ein sehr seltenes Halogenalkan; in der Wikipedia existiert kein Eintrag zu dieser Verbindung, auf einer amerikanischen Webseite findet man, dass es mit "Methoxide ion in methanol" reagiert, und zwar zu "a mixture of (S)-2-fluoro-2-methoxybutane and three fluoroalkenes"[2].
Halothan wird seit 1956 als Betäubungsmittel eingesetzt, ist aber inzwischen von besseren Anästhetika abgelöst worden.
Eigenschaften
Siedepunkte
Vergleicht man die Halogenalkane mit den entsprechenden Alkanen gleicher Molmasse, so findet man, dass die Siedepunkte der Halogenalkane wesenlich höher liegen als die der Alkane:
| Name | molare Masse in g/mol | Siedepunkt in ºC |
| Ethan | 30,07 | -88,6 |
| Fluorethan | 48,06 | -37,1 |
| Chlorethan | 64,15 | 13,1 |
| Bromethan | 108,97 | 38 |
| Iodethan | 155,97 | 71 |
| n-Butan | 58,12 | -0,5 |
| 1-Chlorbutan | 92,57 | 78 |
| 1-Brombutan | 137,03 | 102 |
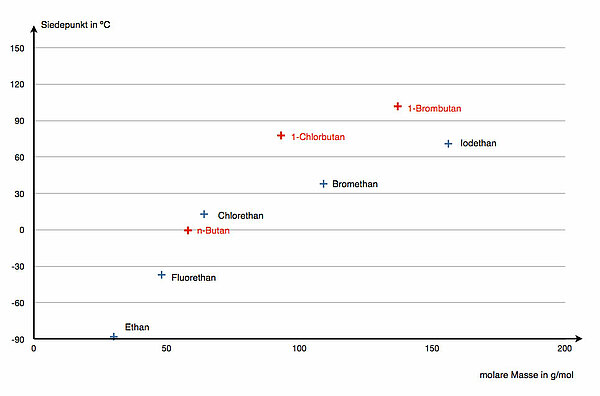
Hier eine entsprechende graphische Darstellung. Auf diesem Bild sieht man gut, dass die Siedepunkt in erster Linie von der molaren Masse der Alkane bzw. Halogenalkane abhängt. Es ist also nicht das Chlor- oder Brom-Atom allein, das den hohen Siedepunkt bewirkt, sondern die Masse des Moleküls hat einen genau so starken Einfluss.
Dennoch ist es natürlich so, dass Halogen-Atome eine hohe Elektronegativität besitzen und somit das Halogenalkan-Molekül polarisieren. H-Brücken können allerdings nicht ausgebildet werden, denn die H-Atome sitzen ja an C-Atomen und nicht an O- oder N-Atomen, wie es für die Ausbildung von Wasserstoffbrücken-Bindungen erforderlich ist. Aber die Halogenalkan-Moleküle sind Dipole, und das erklärt dann die im Vergleich zu den Alkanen höheren Siedepunkt zumindest teilweise.
Den Einfluss der van-der-Waals-Kräfte kann man vielleicht beim Vergleich von Fluorethan und n-Butan sehen. Beide Moleküle haben in etwa die gleiche molare Masse (48 bzw. 58 g/mol), dennoch hat das Butan-Moleküle einen deutlich höheren Siedepunkt als das Fluorethan. Das könnte an den van der Waals-Kräften liegen, die zwischen den langgestreckten n-Butan-Molekülen herrschen. Das Fluorethan ist zwar ein Dipol, jedoch sehr kurzkettig, so dass die van der Waals-Kräfte kaum eine Rolle spielen.
Quellen:
- Römpp Chemie-Lexikon, 9. Auflage 1992
- Webseite zum Lösungsbuch zu "Get Ready for Organic Chemistry" von Leroy G. Wade, ISBN 032183296
- Wikipedia, verschiedene Artikel zu Halogenalkanen