Die gesamte Erde ist in ca. 20 km Höhe von einer Ozonschicht umgeben, die die Lebewesen vor schädlicher UV-Strahlung schützt. Die Ozon-Konzentration in dieser Schicht ist nicht allzu hoch. Durch anthropogene Einflüsse (durch den Menschen verursacht) hat die Ozonkonzentration vor allem über der Antarktis drastisch abgenommen. Diese "Ausdünnung" der Ozonschicht wird jetzt als Ozonloch bezeichnet.

Diese schöne von Adrew Ryhkov erstellte animierte Graphik zeigt, wie sich das Ozonloch in den Jahren 1957 bis 2001 verändert hat.
Ursachen der Ozonzerstörung
Hauptursache der Ausdünnung der Ozonschicht sind vor allem Chlor-Radikale aus Fluorchlorkohlenwasserstoffen (FCKWs).

Ein Chlor-Radikal reagiert mit einem Ozon-Molekül zu einem Molekül Chlormonooxid ClO und einem Sauerstoff-Molekül. Das Chlormonooxid kann dann mit einem Sauerstoff-Radikal zu einem neuen Chlor-Radikal und Sauerstoff reagieren. Das neue Chlor-Radikal kann wieder den ersten Kettenfortpflanzungsschritt durchlaufen und so weiter...
Von diesen beiden Schritten läuft der zweite sehr langsam ab, weil die Konzentration des atomaren Sauerstoffs in der Atmosphäre recht gering ist. Fasst man beide Schritte zusammen, so ergibt sich:
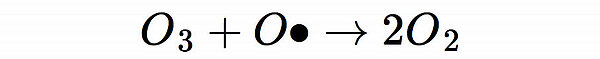
Die Chlor-Radikale nehmen an der Gesamtreaktion im Prinzip nicht teil, wirken also eher als Katalysator, was umso schlimmer ist, da ein einziges Chlor-Radikal zur Vernichtung vieler Tausend Ozon-Moleküle beitragen kann.
Diese Darstellung ist stark vereinfacht, fasst aber die wesentlichen Vorgänge zusammen. Die Reaktion von Chlor mit Ozon ist übrigens eine typische Kettenreaktion, wie bereits oben weiter ausgeführt wurde. Eine für den Unterricht sehr wichtige Kettenreaktion wird in der Stufe Q1 bei der Halogenierung von Alkanen behandelt.