Glycin
Schauen wir uns die Struktur der allereinfachsten Aminosäure an:
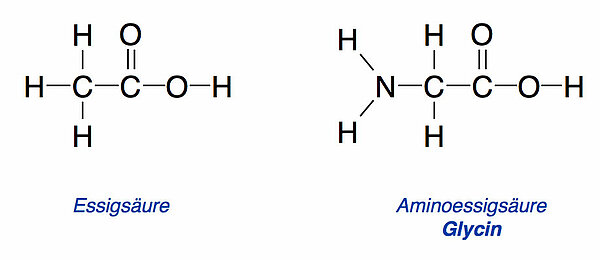
Von den über 20 verschiedenen Aminosäuren, die es gibt, ist Glycin die einfachste Aminosäure. Die Abbildung 1 zeigt die Strukturformel von Glycin. Chemisch vorgebildete Leute erkennen sofort, dass Glycin ein Verwandter der Essigsäure ist. Ein H-Atom der Essigsäure wurde gegen eine Aminogruppe ausgetauscht, insofern kann man Glycin auch als Aminoessigsäure bezeichnen. Somit hat Glycin zwei funktionelle Gruppen. Rechts sieht man die Carboxy- oder COOH-Gruppe, die wir bereits von der Essigsäure und anderen Carbonsäuren kennen, und links sieht man die Amino- oder NH2-Gruppe, die typisch ist für die Stoffgruppe der Amine.
Die Anwesenheit dieser beiden Gruppen verleiht dem Molekül Zwitter-Eigenschaften. Die Carboxy-Gruppe macht Glycin zu einer Säure, denn wie bei allen Carbonsäuren kann die COOH-Gruppe ihr H-Atom als Proton H+ abgeben (Säuren = Protonen-Donatoren). Andererseits macht die Amino-Gruppe das Glycin zu einer Base, denn die Amino-Gruppe kann ein Proton aufnehmen.
Alanin
Kommen wir nun zur nächst komplizierten Aminosäure. Das Alanin sieht fast genau so aus wie das Glycin, allerdings ist eines der beiden H-Atome des zentralen C-Atoms gegen eine Methyl-Gruppe ausgetauscht worden:
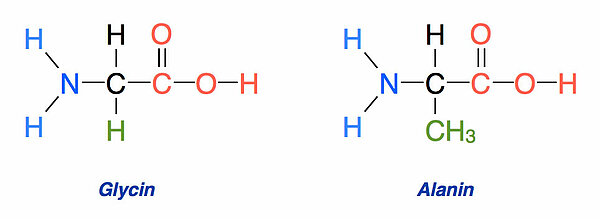
Auf diesem Bild werden die beiden einfachsten Aminosäuren Glycin und Alanin einander gegenübergestellt. Außerdem sind hier die beiden funktionellen Gruppen farbig hervorgehoben: Die Aminogruppe blau und die Carboxygruppe rot.
Das, was die beiden Aminosäuren unterscheidet, wurde grün hervorgehoben. Der sogenannte Aminosäurerest besteht beim Glycin aus einem H-Atom, beim Alanin aus einer Methyl- oder CH3-Gruppe. Oft wird dieser Aminosäurerest auch als Seitengruppe oder Seitenkette bezeichnet.
Die 20 proteinogenen Aminosäuren
In der Natur gibt es viele Aminosäuren, laut dem Spektrum-Lexikon der Biologie über 260[2]. Aber nur 20 davon kommen in den Peptiden und Proteinen der bekannten Lebewesen vor. Diese 20 Aminosäuren werden als proteinogene Aminosäuren bezeichnet. Wörtlich übersetzt: "Aminosäuren, aus denen Proteine entstehen". Die Aminosäuren sind in reinem Zustand farblose kristalline Stoffe, die in festem Zustand überwiegend als Zwitterionen vorliegen[1].
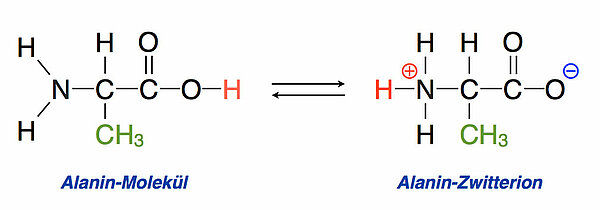
Auf diesem Bild sieht man das Alanin-Molekül und das Alanin-Zwitterion. Beide Formen stehen in einem Gleichgewicht, allerdings liegt das Gleichgewicht dieser internen Protonenübertragung weit auf der rechten Seite, also auf der Seite des Zwitterions.
Nach Römpp (und anderen Quellen) werden die 20 Aminosäuren in vier Gruppen eingeteilt.
Aminosäuren mit unpolaren Seitengruppen
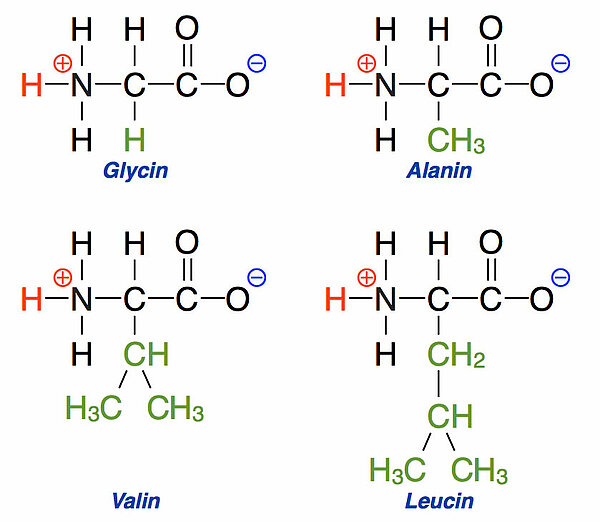
Auch die Aminosäuren Isoleucin, Prolin, Tryptophan, Phenylalanin und Methionin gehören zu den Aminosäuren mit unpolaren Seitenketten. Solche Aminosäuren werden auch einfach als unpolare Aminosäuren bezeichnet. Die Stellung von Glycin ist etwas umstritten. Der Römpp ordnet Glycin bei den Aminosäuren mit polaren Seitenketten ein, das Spektrum-Lexikon der Biologie bei den Aminosäuren mit unpolaren Seitenketten.
Aminosäuren mit polaren ungeladenen Seitenketten
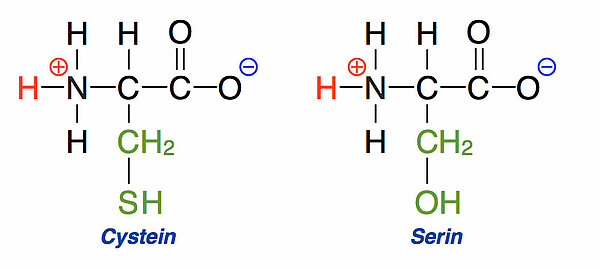
Serin hat eine OH-Gruppe in der Seitenkette. Hydroxygruppen (OH-Gruppen) haben ein stark elektronegatives O-Atom und sind daher recht polar - das kennt man auch von Alkoholen her und natürlich vom Wasser-Molekül, das ja ein starker Dipol ist. Wegen der stark polaren OH-Gruppe ist dann auch die Seitenkette und damit die gesamte Aminosäure polar. Man achte aber darauf, dass in der Seitenkette des Serins keine elektrische Ladung vorkommt. Daher gehört Serin zu den polaren ungeladenen Aminosäuren.
Eng verwandt mit dem Serin ist das Cystein, eine äußerst wichtige Aminosäure, wie wir später noch sehen werden. Hier ist das O-Atom in der Seitenkette durch ein S-Atom ausgetauscht, also ein Schwefel-Atom.
Andere Aminosäuren mit ungeladenen aber polaren Seitenketten sind Tyrosin, Threonin, Asparagin und Glutamin.
Aminosäuren mit negativ geladenen Seitengruppen = saure Aminosäuren
Quellen:
- Römpp Chemie-Lexikon, 9. Auflage 1992, Artikel "Aminosäuren".
- Spektrum Lexikon der Biologie, Artikel "Aminosäuren" 1999